NEWS
NEWS
How mammalian embryos prepare for the first big, irreversible decision
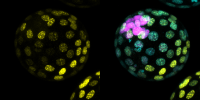
Left: a 64-cell mouse embryo showing CEBPa expression in the nuclei of cells (in yellow), coinciding with the trophectoderm, the outer layer that will eventually form the placenta. Right: image merged with the embryo stained for OCT4 expression (in pink) to indicate the future adult body, and for DNA (in blue/green). Credit: Marcos Plana-Carmona, Centre for Genomic Regulation
Life begins with a single-cell embryo, which divides to form more cells. At some point during these very early days, each cell’s fate must be decided. Some cells will become the inner cell mass, which forms the future adult body. The rest will form the trophectoderm, an outer layer that will eventually transform into the placenta, a tissue that sustains the embryo as it grows.
Whether a cell ends up becoming the inner cell mass or trophectoderm is the first big decision in embryonic life. It usually happens around the 16-cell stage and represents a point of no return.
Understanding the fundamental principles of this first big decision can help shed light on how embryos form, their placenta develops, how they implant into the womb, and why some embryos fail to progress. A study published today in Science Advances shows how mouse early embryonic cells acquire the ability to make the first cell fate choice in development.
Researchers at the Centre for Genomic Regulation (CRG) in Barcelona and the University of Cambridge in the UK show there is no binary switch where cells suddenly choose their fate. Instead, they prepare for several futures at once before committing to any of them at the sixteen-cell stage.
“We found that cells don’t suddenly decide what fate to acquire but begin to prime themselves much earlier, at the transition to the four-cell stage,” says Dr. Magdalena Zernicka Goetz, senior co-author and researcher at Cambridge University and now at the California Institute of Technology. “This helps explain how early life builds the foundations of the body.”
How embryos get prepared while also keeping options open
The authors of the study found that CEBPa, a protein that turns genes on or off, also known as a transcription factor, is a key orchestrator. It is expressed transiently before the first bifurcation in the embryo, making a collection of regulatory sequences accessible when active.
When researchers forced embryonic stem cells to make CEBPa, they learned that both the amount of CEBPa and how long it is present matter. If cells only see a little CEBPa, or see it for a short time, they start to look a bit like trophectoderm cells but can still go back to being pluripotent once CEBPa is removed. This appears to be similar to what happens in real embryos, where CEBPa is only switched on at the two-cell to four-cell stage transition before the first major fate decision.
The study also found which regulatory sequences, stretches of DNA that control other genes, are controlled by CEBPa. Many of these regulatory sequences are critical for the expression of trophectoderm fate genes (Tead4, Gata3, Cdx2, Elf5) and are already open in four to eight-cell mouse embryos.
The findings are important because they suggest that early embryos do not wait until fate is decided to remodel their genome, but rather establish a landscape in which trophectoderm genes can be activated rapidly once the right signal arrives.
“CEBPa is working like an architect of future responsiveness in this scenario, helping embryos keep several doors slightly ajar until the moment of choice,” explains Dr. Thomas Graf, senior author of the publication at the Centre for Genomic Regulation.
The study adds weight to the multilineage priming hypothesis, a theory that posits that uncommitted cells express genetic programmes associated with multiple fates before deciding. In other words, stem cells anticipate instructions while keeping their options open before making their first irreversible choice.
Relevance beyond mice
These findings shed light on the rules governing mammalian development, which can also help us understand the earliest chapters of our own biology. However, as they were made in mice, claims about human applications are limited.
The authors of the study found that, as in mice, CEBPa is also specifically expressed in the trophectoderm layer of human blastocysts, although they note that human embryos donated for research are not accessible to examine a potential role of this factor in the earliest stages of life.
Strikingly, human embryos express the transcription factor at later stages than mouse embryos. This may reflect the fact that the genomes of human zygotes aren’t activated until the 8-cell stage, whereas those of mice are activated at the 2-cell stage. This means that human embryos may not be able to express priming factors until later in development.
And while we lack human embryo datasets, studies of human embryonic stem cells have shown that overexpressing CEBPa activates trophectoderm genes. It implies the human genome also responds to CEBPa, though the timing may be shifted in comparison to mice.
EN CASTELLANO
Cómo los embriones de los mamíferos se preparan para su primera gran decisión irreversible
La vida comienza con un embrión unicelular, que se divide para formar más células. En algún momento de estos primeros días, debe decidirse el destino de cada célula. Algunas se convertirán en la masa celular interna, que dará lugar al futuro cuerpo adulto. El resto formará el trofectodermo, una capa externa que acabará transformándose en la placenta, un tejido que sostiene al embrión a medida que crece.
Que una célula termine formando la masa celular interna o el trofectodermo constituye la primera gran decisión en la vida embrionaria. Suele producirse en torno al estadio de 16 células y representa un punto de no retorno.
Comprender los principios fundamentales de esta primera gran decisión puede ayudar a esclarecer cómo se forman los embriones, cómo se desarrolla su placenta, cómo se implantan en el útero y por qué algunos dejan de progresar. Un estudio publicado hoy en Science Advances muestra cómo las células embrionarias tempranas de ratón adquieren la capacidad de tomar la primera decisión del destino celular durante el desarrollo.
Investigadores del Centro de Regulación Genómica (CRG), en Barcelona, y de la Universidad de Cambridge, en el Reino Unido, señalan que no existe un interruptor binario mediante el cual las células elijan repentinamente su destino. En su lugar, se preparan para varios futuros simultáneamente antes de comprometerse con alguno de ellos en el estadio de dieciséis células.
“Observamos que las células no deciden de repente qué destino adquirir, sino que comienzan a prepararse mucho antes, en la transición al estadio de cuatro células”, afirma la Dra. Magdalena Zernicka-Goetz, coautora sénior del estudio e investigadora en la Universidad de Cambridge y actualmente en el Instituto Tecnológico de California. “Esto ayuda a explicar cómo la vida temprana construye los cimientos del cuerpo”.
Cómo se preparan los embriones mientras mantienen abiertas sus opciones
Los autores del estudio descubrieron que CEBPa, una proteína que activa o desactiva genes —un factor de transcripción—, actúa como un elemento clave. Se expresa de forma transitoria antes de la primera bifurcación del embrión, haciendo accesible un conjunto de secuencias reguladoras mientras está activa.
Cuando los investigadores forzaron a las células madre embrionarias a producir CEBPa, se observó que tanto la cantidad de esta proteína como el tiempo durante el que está presente resultan determinantes. Si las células solo reciben una cantidad reducida de CEBPa, o la perciben durante un periodo breve, comienzan a parecer células de trofectodermo, pero pueden volver a ser pluripotentes una vez que CEBPa se retira. Esto parece ser similar a lo que sucede en los embriones reales, donde CEBPa solo se activa en la transición del estadio de dos a cuatro células antes de la primera gran decisión del destino.
El estudio también identificó qué secuencias reguladoras —tramos de ADN que controlan otros genes— están reguladas por CEBPa. Muchas de estas secuencias son cruciales para la expresión de genes del trofectodermo (Tead4, Gata3, Cdx2, Elf5) y ya se encuentran abiertas en embriones de ratón de cuatro a ocho células.
Los resultados son relevantes porque sugieren que los embriones tempranos no esperan a que se decida el destino celular para remodelar su genoma, sino que establecen un paisaje en el que los genes del trofectodermo pueden activarse rápidamente cuando llega la señal adecuada.
“En este escenario, CEBPa actúa como un arquitecto de la capacidad de respuesta futura, ayudando a los embriones a mantener varias puertas entreabiertas hasta el momento de la elección”, explica el Dr. Thomas Graf, autor sénior de la publicación en el Centro de Regulación Genómica.
El estudio refuerza la hipótesis del multilineage priming, una teoría que sostiene que las células no comprometidas expresan programas genéticos asociados a múltiples destinos antes de decidirse. En otras palabras, las células madre anticipan las instrucciones mientras mantienen abiertas sus opciones antes de realizar su primera elección irreversible.
Relevancia más allá del ratón
Estos resultados ayudan a esclarecer las normas que rigen el desarrollo de los mamíferos, lo que también puede contribuir a entender los capítulos más tempranos de nuestra propia biología. Sin embargo, dado que se obtuvieron en ratones, las afirmaciones sobre aplicaciones humanas son limitadas.
Los autores del estudio descubrieron que, al igual que en los ratones, CEBPa también se expresa específicamente en la capa de trofectodermo de los blastocitos humanos, si bien señalan que los embriones humanos donados para investigación no son accesibles para examinar una posible función de este factor en las etapas más tempranas de la vida.
Resulta llamativo que los embriones humanos expresen este factor de transcripción en fases más tardías que los embriones de ratón. Esto podría reflejar el hecho de que el genoma de los cigotos humanos no se activa hasta el estadio de ocho células, mientras que el de los ratones se activa en el estadio de dos células. Esto significa que los embriones humanos podrían no ser capaces de expresar factores de preparación hasta fases más avanzadas del desarrollo.
Y aunque no se dispone de conjuntos de datos de embriones humanos, estudios realizados con células madre embrionarias humanas han demostrado que la sobreexpresión de CEBPa activa genes del trofectodermo. De ello se desprende que el genoma humano también responde a CEBPa, aunque el momento de dicha respuesta podría diferir respecto al de los ratones.
EN CATALÀ
Com els embrions dels mamífers es preparen per a la seva primera gran decisió irreversible
La vida comença amb un embrió unicel·lular, que es divideix per formar més cèl·lules. En algun moment d'aquests primers dies, s'ha de decidir el destí de cada cèl·lula. Algunes es convertiran en la massa cel·lular interna, que donarà lloc al futur cos adult. La resta formarà el trofectoderma, una capa externa que acabarà transformant-se en la placenta, un teixit que sosté l'embrió a mesura que creix.
Que una cèl·lula acabi formant la massa cel·lular interna o el trofectoderma constitueix la primera gran decisió en la vida embrionària. Sol produir-se al voltant de l'estadi de 16 cèl·lules i representa un punt de no retorn.
Comprendre els principis fonamentals d'aquesta primera gran decisió pot ajudar a aclarir com es formen els embrions, com es desenvolupa la seva placenta, com s'implanten a l'úter i per què alguns deixen de progressar. Un estudi publicat avui a Science Advances mostra com les cèl·lules embrionàries primerenques de ratolí adquireixen la capacitat de prendre la primera decisió del destí cel·lular durant el desenvolupament.
Investigadors del Centre de Regulació Genòmica (CRG), a Barcelona, i de la Universitat de Cambridge, al Regne Unit, assenyalen que no existeix un interruptor binari mitjançant el qual les cèl·lules trien sobtadament el seu destí. Ans al contrari, es preparen per a diversos futurs simultàniament abans de comprometre's amb algun d'ells a l'estadi de setze cèl·lules.
"Observem que les cèl·lules no decideixen de sobte quin destí adquirir, sinó que comencen a preparar-se molt abans, en la transició a l'estadi de quatre cèl·lules", afirma la Dra. Magdalena Zernicka-Goetz, coautora sènior de l’estudi i investigadora de la Universitat de Cambridge i actualment a l’Institut Tecnològic de Califòrnia. "Això ajuda a explicar com la vida primerenca construeix els fonaments del cos".
Com es preparen els embrions mentre mantenen obertes les seves opcions
Els autors de l'estudi van descobrir que CEBPa, una proteïna que activa o desactiva gens —un factor de transcripció—, actua com a element clau. S'expressa de forma transitòria abans de la primera bifurcació de l'embrió, fent accessible un conjunt de seqüències reguladores mentre està activa.
Quan els investigadors van forçar les cèl·lules mare embrionàries a produir CEBPa, es va observar que tant la quantitat d'aquesta proteïna com el temps durant el qual està present resulten determinants. Si les cèl·lules només reben una quantitat reduïda de CEBPa, o la perceben durant un període breu, comencen a semblar cèl·lules de trofectoderma, però poden tornar a ser pluripotents una vegada que CEBPa es retira. Això és semblant al que succeeix en els embrions reals, on CEBPa només s'activa en la transició de l'estadi de dues a quatre cèl·lules, abans de la primera gran decisió del destí.
L'estudi també va identificar quines seqüències reguladores —trams d'ADN que controlen altres gens— estan regulades per CEBPa. Moltes d'aquestes seqüències són crucials per a l'expressió de gens del trofectoderma (Tead4, Gata3, Cdx2, Elf5) i ja es troben obertes en embrions de ratolí de quatre a vuit cèl·lules.
Els resultats són rellevants perquè suggereixen que els embrions primerencs no esperen que es decideixi el destí cel·lular per remodelar el seu genoma, sinó que estableixen un paisatge en el qual els gens del trofectoderma poden activar-se ràpidament quan arriba el senyal adequat.
"En aquest escenari, CEBPa actua com un arquitecte de la capacitat de resposta futura, ajudant els embrions a mantenir diverses portes entreobertes fins al moment de l'elecció", explica el Dr. Thomas Graf, autor sènior de la publicació al Centre de Regulació Genòmica.
L'estudi reforça la hipòtesi del multilineage priming, una teoria que sosté que les cèl·lules no compromeses expressen programes genètics associats a múltiples destinacions abans de decidir-se. En altres paraules, les cèl·lules mare anticipen les instruccions mentre mantenen obertes les seves opcions abans de realitzar la seva primera elecció irreversible.
Rellevància més enllà del ratolí
Aquests resultats ajuden a aclarir les normes que regeixen el desenvolupament dels mamífers, la qual cosa també pot contribuir a entendre els capítols més primerencs de la nostra pròpia biologia. Tanmateix, atès que es van obtenir en ratolins, les afirmacions sobre aplicacions humanes són limitades.
Els autors de l'estudi van descobrir que, igual que en els ratolins, CEBPa també s'expressa específicament en la capa de trofectoderma dels blastòcits humans, si bé assenyalen que els embrions humans donats per a la recerca no són accessibles per examinar una possible funció d'aquest factor en les etapes més primerenques de la vida.
Resulta curiós que els embrions humans expressin aquest factor de transcripció en fases més tardanes que els embrions de ratolí. Això podria reflectir el fet que el genoma dels zigots humans no s'activa fins a l'estadi de vuit cèl·lules, mentre que el dels ratolins s'activa a l'estadi de dues cèl·lules. Això significa que els embrions humans podrien no ser capaços d'expressar factors de preparació fins a fases més avançades del desenvolupament.
I tot i que no es disposa de conjunts de dades d'embrions humans, estudis realitzats amb cèl·lules mare embrionàries humanes han demostrat que la sobreexpressió de CEBPa activa gens del trofectoderma. D'això se'n desprèn que el genoma humà també respon a CEBPa, tot i que el moment d'aquesta resposta podria diferir respecte al dels ratolins.