NEWS
NEWS
MiOS captures how genes fold and work at unprecedented resolution
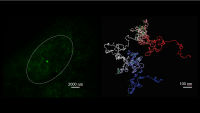
Comparison using a conventional microscope (left) to visualise the structure of NANOG gene, which shows up as a bright green spot vs. using MiOS (right) which can image individual genes. MiOS is roughly ten times better resolution and also details critical aspects of the structure that are not discernible using conventional methods. Credit: Vicky Neguembor/CRG and Pablo Dans/IRB Barcelona
A new imaging technique captures the structure of the human genome at unprecedented resolution, revealing how individual genes fold at the nucleosome level – the fundamental units constituting the genome’s three-dimensional architecture.
Developed by Barcelona-based researchers at the Centre for Genomic Regulation (CRG) and the Institute for Research in Biomedicine (IRB Barcelona), the technique works by combining high-resolution microscopy and advanced computational modelling. It is the most comprehensive method created to date to study the shape of genes.
Researchers can use the new technology to create and virtually navigate three-dimensional models of genes, visualizing not only their structures but providing details on how they move or how flexible they are. Because almost every human disease has some basis in genes, understanding how they work could lead to a deeper understanding on how they affect the human body in both health and disease.
Eventually, scientists can use this information to predict what happens to genes when things go wrong, for example by cataloguing variations in the shape of genes that cause disease. The technology could also be used to test drugs that change the shape of an aberrant gene, helping discover new treatments for different types of disease.
The technology is the next evolution of imaging techniques used to study living organisms, which first started more than four hundred years ago with the creation of microscopes. These played a crucial role in advancing medicine and human health, for example used by Robert Hooke to describe cells for the first time and later used by Santiago Ramón y Cajal to identify neurons. Despite great advances, the limitations of optical microscopes were clear as far back as 1873, with researchers stipulating that their maximum resolution could not surpass 0.2 micrometres.
This physical limit was overcome in the 21st century with the creation of super-resolution microscopy, a breakthrough which was awarded the Nobel Prize in Chemistry in 2014. Using fluorescence, researchers extended the limits of light microscopy and captured events at 20 nanometres, a feat that revealed how life works at unprecedented molecular scale.
Super-resolution microscopy changed the course of biomedical research, enabling scientists to track proteins in a variety of diseases. It also enabled researchers to study molecular events that regulate gene expression. Scientists now want to build on the technology and take it one step further by adding more layers of information.
Researchers hypothesised that taking super-resolution microscopy and merging it with advanced computational tools could be a way of imaging genes at the level of detail necessary to study their shape and function. An interdisciplinary team of scientists shared their expertise and created a new technique called Modeling immuno-OligoSTORM – or MiOS for short.
The two research groups teamed up as part of the Barcelona Institute of Science and Technology’s (BIST) Ignite Call, which facilitates the exchange of knowledge among different scientific fields and exploring new approaches to address complex questions.
"Our computational modelling strategy integrates data from DNA sequencing techniques and super-resolution microscopy to provide an essential picture (or movie) of the 3D shape of genes at resolutions beyond the size of nucleosomes, reaching the scales needed to understand in detail the interaction between chromatin and other cell factors," says Dr. Juan Pablo Arcon, co-first author of the work and postdoctoral researcher at IRB Barcelona.
As proof of concept, the research team used MiOS to provide new insights on the position, shape and compaction of key housekeeping and pluripotency genes, revealing new structures and details that are not captured using conventional techniques alone. The findings are published today in the journal Nature Structural & Molecular Biology. The study's corresponding authors are ICREA Research Professor Pia Cosma at the CRG and Professor Modesto Orozco at IRB Barcelona, as well as Pablo Dans, previously a researcher at IRB Barcelona and now at University of the Republic (Uruguay) and the Institut Pasteur of Montevideo.
“We show that MiOS provides unprecedented detail by helping researchers virtually navigate inside genes, revealing how they are organised at a completely new scale. It is like upgrading from the Hubble Space Telescope to the James Webb, but instead of seeing distant stars we’ll be exploring the farthest reaches inside a human nucleus,” says Dr. Vicky Neguembor, co-first and co-corresponding author of the study and researcher at the CRG.
While a lot of genome-based research is already changing how we diagnose, treat or prevent diseases, the impact of MiOS is more long-term. By shedding light on how genes work and how they are regulated at the nanoscale, the technique will enable new discoveries in the scientific laboratory, some of which might eventually translate into clinical practice.
The research team is already putting MiOS to use by exploring genes that are important for human development. The team will also keep developing MiOS further, adding additional functionality that can for example detect how transcription factors – proteins involved in the process of converting, or transcribing, DNA into RNA – bind to DNA.
EN CASTELLANO
Una nueva técnica captura cómo los genes se pliegan y funcionan a una resolución sin precedentes
Una nueva técnica de imagen captura la estructura del genoma humano a una resolución sin precedentes, revelando cómo los genes individuales se pliegan a nivel de nucleosomas – las unidades fundamentales que constituyen la arquitectura tridimensional del genoma.
La técnica, desarrollada por un equipo científico barcelonés del Centro de Regulación Genómica (CRG) y del Instituto de Investigación Biomédica (IRB Barcelona), funciona combinando la microscopía de alta resolución y la modelización computacional avanzada. Es el método más minucioso creado hasta la fecha para estudiar la forma de los genes.
Ahora, los investigadores pueden usar la nueva tecnología para crear modelos tridimensionales de genes y navegarlos virtualmente, visualizando no solo sus estructuras, sino también proporcionando detalles sobre cómo se mueven o cuán flexibles son. Debido a que casi todas las enfermedades humanas tienen alguna base en los genes, comprender cómo funcionan podría conducir a una comprensión más profunda de cómo afectan al cuerpo humano tanto en la salud como en la enfermedad.
A la larga, se podrá usar esta información para predecir lo que sucede con los genes cuando las cosas van mal, por ejemplo, catalogando las variaciones en la forma de los genes que causan enfermedades. La tecnología también podría usarse para probar fármacos que cambian la forma de un gen aberrante, ayudando a descubrir nuevos tratamientos para diferentes tipos de enfermedades.
La tecnología es la próxima evolución de las técnicas de imagen utilizadas para estudiar los organismos vivos, que comenzó hace más de cuatrocientos años con la creación de los microscopios. Estos jugaron un papel crucial en el avance de la medicina y la salud humana, por ejemplo, utilizados por Robert Hooke para describir las células por primera vez y luego utilizados por Santiago Ramón y Cajal para identificar las neuronas. A pesar de los grandes avances, las limitaciones de los microscopios ópticos eran claras desde el 1873, cuando se estipuló que la resolución máxima no podía superar los 0,2 micrómetros.
Este límite físico se superó en el siglo XXI con la creación de la microscopía de superresolución, un gran avance que fue galardonado con el Premio Nobel de Química en 2014. Usando la fluorescencia, los investigadores extendieron los límites de la microscopia, capturando eventos a 20 nanómetros, una hazaña que reveló cómo funciona la vida a una escala molecular sin precedentes.
La microscopía de superresolución cambió el curso de la investigación biomédica, permitiendo a la ciencia rastrear las proteínas en una variedad de enfermedades. También permitió el estudio de los eventos moleculares que regulan la expresión génica. Ahora la ciencia busca llevar la tecnologia un paso más allá, agregando más capas de información.
El equipo científico planteó la hipótesis de que usando la microscopía de superresolución y fusionándola con herramientas computacionales avanzadas se podría obtener imágenes de genes al nivel de detalle necesario para estudiar su forma y función. El equipo interdisciplinario de científicos compartió su experiencia y creó una nueva técnica llamada Modeling immuno-OligoSTORM – o MiOS para abreviar.
Los dos grupos de investigación se unieron en el marco de la Convocatoria Ignite del Barcelona Institute of Science and Technology (BIST), que facilita el intercambio de conocimientos entre diferentes campos científicos y la exploración de nuevos enfoques para abordar cuestiones complejas.
"Nuestra estrategia de modelado computacional integra datos de técnicas de secuenciación de ADN y microscopía de superresolución para proporcionar una imagen (o película) esencial de la forma 3D de los genes a resoluciones más allá del tamaño de los nucleosomas, alcanzando las escalas necesarias para comprender en detalle la interacción entre la cromatina y otros factores celulares", dice el Dr. Juan Pablo Arcon, co-primer autor del trabajo e investigador postdoctoral en el IRB Barcelona.
Como prueba de concepto, el equipo de investigación utilizó MiOS para proporcionar nuevos conocimientos sobre la posición, la forma y la compactación de genes clave de ‘housekeeping’ y pluripotencia, revelando nuevas estructuras y detalles que no se capturan utilizando solo técnicas convencionales. Los hallazgos se publican hoy en la revista Nature Structural & Molecular Biology. Los autores principales del estudio incluyen la profesora de investigación ICREA Pia Cosma en el CRG, el profesor Modesto Orozco en el IRB Barcelona y Pablo Dans, previamente investigador en el IRB Barcelona y actualmente en la Universidad de la República (Uruguay) y el Institut Pasteur de Montivideo.
"Demostramos que MiOS proporciona detalles sin precedentes, ayudándonos navegar virtualmente dentro de los genes y revelando cómo están organizados a una escala completamente nueva. Es como actualizar del Telescopio Espacial Hubble al James Webb, pero en lugar de ver estrellas distantes exploraremos los confines más lejanos dentro de un núcleo humano", afirma la Dra. Vicky Neguembor, co-primera autora del estudio e investigadora del CRG.
Si bien una gran cantidad de descubrimientos científicos sobre el genoma ya están cambiando la forma en que diagnosticamos, tratamos o prevenimos las enfermedades, el impacto de MiOS será más a largo plazo. Al arrojar luz sobre el funcionamiento y la regulación de los genes a nanoescala, la técnica permitirá nuevos descubrimientos en el laboratorio científico, algunos de los cuales finalmente podrían traducirse en la práctica clínica.
El equipo de investigación ya está utilizando MiOS para explorar genes importantes para el desarrollo humano. Además, el equipo seguirá desarrollando MiOS, agregando funcionalidades adicionales que puedan, por ejemplo, detectar cómo los factores de transcripción (proteínas involucradas en el proceso de conversión o transcripción de ADN en ARN) se unen al ADN.
EN CATALÀ
Una nova tècnica captura com els gens es pleguen i funcionen a una resolució sense precedents
Una nova tècnica d'imatge captura l'estructura del genoma humà a una resolució sense precedents i revela com els gens individuals es pleguen a nivell dels nucleosomes – les unitats fonamentals que constitueixen l'arquitectura tridimensional del genoma.
La tècnica desenvolupada per un equip científic barceloní del Centre de Regulació Genòmica (CRG) i l'Institut de Recerca Biomèdica (IRB Barcelona) funciona combinant la microscòpia d'alta resolució i la modelització computacional avançada. És el mètode més acurat creat fins ara per estudiar la forma dels gens.
Ara, els investigadors poden utilitzar la nova tecnologia per crear models tridimensionals de gens i navegar-los virtualment, visualitzant-ne no només les estructures, sinó també proporcionant detalls sobre com es mouen o com de flexibles són. Com que gairebé totes les malalties humanes tenen alguna base als gens, comprendre com funcionen podria conduir a una comprensió més profunda de com afecten el cos humà tant en la salut com en la malaltia.
A la llarga, es podrà fer servir aquesta informació per predir el que passa amb els gens quan les coses van malament, per exemple, catalogant les variacions en la forma dels gens que causen malalties. La tecnologia també es podria fer servir per provar fàrmacs que canvien la forma d'un gen aberrant, ajudant a descobrir nous tractaments per a diferents tipus de malalties.
La tecnologia és la propera evolució de les tècniques d'imatge utilitzades per estudiar els organismes vius, que va començar fa més de quatre-cents anys amb la creació dels microscopis. Aquests van jugar un paper crucial en l'avenç de la medicina i la salut humana, per exemple, utilitzats per Robert Hooke per descriure les cèl·lules per primera vegada i després utilitzats per Santiago Ramón i Cajal per identificar les neurones. Tot i els grans avenços, les limitacions dels microscopis òptics eren clares des del 1873, quan es va estipular que la resolució màxima no podia superar els 0,2 micròmetres.
Aquest límit físic es va superar al segle XXI amb la creació de la microscòpia de superresolució, un gran avenç que va ser guardonat amb el Premi Nobel de Química el 2014. Usant la fluorescència, els investigadors van estendre els límits de la microscòpia, capturant esdeveniments a 20 nanòmetres, una gesta que va revelar com funciona la vida a una escala molecular sense precedents.
La microscòpia de superresolució va canviar el curs de la investigació biomèdica, permetent a la ciència rastrejar les proteïnes en una varietat de malalties. També va permetre estudiar els esdeveniments moleculars que regulen l'expressió gènica. Ara la ciència busca portar la tecnologia un pas més enllà, afegint-hi més capes d'informació.
L'equip científic va plantejar la hipòtesi que fent servir la microscòpia de superresolució i fusionant-la amb eines computacionals avançades es podrien obtenir imatges dels gens al nivell de detall necessari per estudiar-ne la forma i la funció. L'equip interdisciplinari de científics va compartir la seva experiència i va crear una nova tècnica anomenada Modeling immuno-OligoSTORM – o MiOS per abreujar.
Els dos grups de recerca es van unir en el marc de la Convocatòria Ignite del Barcelona Institute of Science and Technology (BIST), que facilita l'intercanvi de coneixements entre diferents camps científics i l'exploració de nous enfocaments per abordar qüestions complexes.
"La nostra estratègia de modelatge computacional integra dades de tècniques de seqüenciació d'ADN i microscòpia de superresolució per proporcionar una imatge (o pel·lícula) essencial de la forma 3D dels gens a resolucions més enllà de la mida dels nucleosomes, aconseguint les escales necessàries per comprendre en detall la interacció entre la cromatina i altres factors cel·lulars”, diu el Dr. Juan Pablo Arcon, co-primer autor del treball i investigador postdoctoral a l'IRB Barcelona.
Com a prova de concepte, l'equip de recerca va utilitzar MiOS per proporcionar nous coneixements sobre la posició, la forma i la compactació de gens clau de housekeeping i pluripotència, revelant noves estructures i detalls que no es capturen utilitzant només tècniques convencionals. Les troballes es publiquen avui a la revista Nature Structural & Molecular Biology. Els autors principals de l'estudi inclouen la professora de recerca ICREA Pia Cosma al CRG, el professor Modesto Orozco a l'IRB Barcelona i Pablo Dans, prèviament investigador a l'IRB Barcelona i actualment a la Universitat de la República (Uruguai) i l'Institut Pasteur de Montivideo.
"Demostrem que MiOS proporciona detalls sense precedents, ajudant-nos a navegar virtualment dins dels gens i revelant com estan organitzats a una escala completament nova. És com actualitzar del Telescopi Espacial Hubble al James Webb, però en lloc de veure estrelles distants explorarem els confins més llunyans dins d'un nucli humà", afirma la Dra. Vicky Neguembor, co-primera autora de l'estudi i investigadora del CRG.
Si bé una gran quantitat de descobriments científics sobre el genoma ja estan canviant la manera com diagnostiquem, tractem o prevenim les malalties, l'impacte de MiOS serà més a llarg termini. Al posar llum sobre el funcionament i la regulació dels gens a nanoescala, la tècnica permetrà nous descobriments al laboratori científic, alguns dels quals finalment podrien traduir-se a la pràctica clínica.
L'equip de recerca ja fa servir MiOS per explorar gens importants per al desenvolupament humà. A més, l'equip continuarà desenvolupant MiOS, afegint funcionalitats addicionals que puguin, per exemple, detectar com els factors de transcripció (proteïnes involucrades en el procés de conversió o transcripció d'ADN a ARN) s'uneixen a l'ADN.