NEWS
NEWS
Cell division enzyme earmarked as potential new cancer therapeutic target
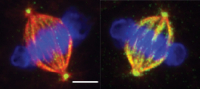
Mitotic spindles with microtubules (red) attached to chromosomes (blue) during cell division. Cells with normal TTLL11 function (right) have normal rates of microtubule polyglutamylation (green) while cells without TTLL11 (left) are unmodified.
- Researchers have identified an enzyme which protects cells from making errors during cell division by ensuring chromosomes are properly segregated
- The enzyme’s activity was found to be compromised in human cancer cells, paving the way for future research to explore whether cancer exploits the mechanism to grow
- The study, published in Nature Communications by researchers at the Centre for Genomic Regulation (CRG), paves the way for further work to explore whether targeting the enzyme is a potentially viable therapeutic option in cancer
When cell division goes wrong, it can lead to the creation of new cells with an abnormal number of chromosomes, a phenomenon known as aneuploidy. The frequency at which chromosome segregation errors occur is known as chromosomal instability (CIN). In some cases, for example a developing embryo, this can promote spontaneous abortion and in others, it can contribute to human diseases such as cancer. Aneuploidy and CIN are hallmarks of particularly aggressive tumours.
Researchers study cell division to understand how chromosome segregation occurs without mistakes every time a cell divides. They also investigate why and how mistakes can occur and generate aneuploid cells.
Faithful chromosome segregation is fully dependent on the correct attachment of the chromosomes to the mitotic spindle, the molecular machinery that pulls chromosomes to opposite sides of a cell. The spindle is formed of microtubules, long-hollow tubes made from proteins. Microtubules must remain stable enough to move and align the chromosomes, but also dynamic enough to allow for correction of the erroneous attachments before chromosomes are pulled apart and segregated.
The dynamics of microtubules and how they are finely regulated are fundamental to understanding how cells divide. Their importance is underscored by the identification of a compound in the early 1970s that is still currently used in chemotherapy and directly stabilizes microtubules, causing cancer cells to self-destruct.
For ICREA Research Professor Isabelle Vernos, Group Leader in the Quantitative Cell Biology research programme at the Centre for Genomic Regulation (CRG), how microtubule dynamics is regulated during cell division in cancer is still not fully understood and could reveal new mechanisms to exploit. Her latest study, published last week in Nature Communications, reveals potential new viable therapeutic targets in cancer.
Microtubules undergo various modifications in different cell types and tissues that finely define their specific functions. In this work, the researchers identified tubulin tyrosine ligase like 11, also known as TTLL11, an enzyme that specifically modifies the spindle microtubules by adding glutamate chains to the surface of the microtubule. This is a process known as polyglutamylation,
They found that microtubule polyglutamylation defines the dynamism and stability of the spindle microtubules, which in turn secure the faithful segregation of the chromosomes. Time-lapse imaging revealed that without TTLL11, cells and zebrafish embryos were much more likely to undergo chromosome segregation errors.
When the researchers examined TTLL11 levels in cancer compared to healthy tissue using data from the Cancer Genome Atlas, a public database that includes molecular characteristics of more than 20,000 primary cancer matched with normal samples spanning 33 cancer types, they found that TTLL11 was significantly downregulated in every single one of these tumours compared to the corresponding normal tissue.
“We found that low levels of TTLL11 are highly specific to cancer. This is exciting because it reveals another layer to how microtubules are regulated during cell division in cancer. Drugs that interfere with microtubule dynamics are already one of the most successful first-line cancer therapies. If this turns out to be a viable therapeutic target, our findings pave the way to the creation of a new generation of drugs that are more precise and effective than conventional treatments,” says Dr. Vernos.
The authors of the study also explained why low levels of TTLL11 affect cell division. “Microtubules need to establish stable connections with the chromosomes to align them and pull them apart, but these connections also need to be flexible enough to be corrected on time to avoid any errors during segregation. Microtubules in cancer cells have low levels of TTLL11, making them too stable thereby favouring the segregation of chromosomes in the presence of attachment errors that will result in aneuploid cells. It remains to be demonstrated whether this is a mechanism being exploited by cancer cells to grow and generate diversity through random chromosome segregation errors. This constitutes new exciting avenues of research,” explains Dr. Vernos.
The research is published in Nature Communications, and is led by first author Ivan Zadra and corresponding author Dr. Isabelle Vernos at the CRG. Collaborators include ICREA Research Professors Dr. Verena Ruprecht and Dr. Luis Serrano, also at the CRG, as well as Carsten Janke at Institut Curie. Other authors include Senda Jimenez, Miquel Anglada, Carolina Segura and Zachary Compton.
EN CASTELLANO
Una enzima del proceso de división celular identificada como potencial nueva diana terapéutica para el cáncer
- Un equipo científico ha identificado una enzima que evita que las células cometan errores durante la división celular, garantizando que los cromosomas puedan separarse correctamente
- La investigación ha descubierto que la actividad de la enzima está comprometida en las células cancerosas humanas, allanando el camino para que futuras investigaciones exploren si el cáncer se aprovecha del mecanismo para crecer
- El equipo científico del CRG, que publica los resultados del estudio en Nature Communications, llevará a cabo futuros estudios para saber si la enzima es una posible diana terapéutica viable en el cáncer
Para crear nuevas células, las existentes deben dividirse. Este es un proceso continuo, frecuente y ubicuo que comienza en la concepción y termina con la muerte. Se estima que hay 37 billones de células en los tejidos y órganos del cuerpo humano, cada una de las cuales se origina a partir de una célula que se divide en dos.
Cuando la división celular falla, puede provocar la creación de nuevas células con un número anormal de cromosomas, un fenómeno conocido como aneuploidía. La frecuencia con la que se producen los errores de segregación cromosómica se conoce como inestabilidad cromosómica (CIN). En algunos casos, por ejemplo, en un embrión en desarrollo, esto puede promover el aborto espontáneo y en otros, puede contribuir a enfermedades humanas como el cáncer. La aneuploidía y la CIN son rasgos comunes en los tumores particularmente agresivos.
Se estudia la división celular para comprender cómo se produce la segregación cromosómica sin errores cada vez que una célula se divide. También se investiga por qué y cómo pueden producirse los errores que generan las células aneuploides.
Una segregación cromosómica fiel depende totalmente de la unión correcta entre los cromosomas y el huso mitótico, la maquinaria molecular que empuja los cromosomas hacia los extremos opuestos de una célula. El huso está formado por microtúbulos, tubos huecos largos formados por proteínas. Los microtúbulos deben permanecer lo suficientemente estables para mover y alinear los cromosomas, pero también lo suficientemente dinámicos para permitir la corrección de las uniones erróneas antes de que los cromosomas se separen y se segreguen.
Esta dinámica de los microtúbulos y su precisa regulación son procesos fundamentales para comprender cómo se dividen las células. Su importancia se destaca por la identificación de un compuesto a principios de la década de 1970 que todavía se usa actualmente en la quimioterapia. El tratamiento estabiliza directamente los microtúbulos, lo que hace que las células cancerosas se autodestruyan.
Para la Profesora de Investigación ICREA Isabelle Vernos, jefa de grupo en el programa de investigación de Biología Celular Cuantitativa en el Centro de Regulación Genómica (CRG), aún no se comprende completamente cómo se regula la dinámica de los microtúbulos durante la división celular en el cáncer. Una mayor comprensión podría revelar nuevos mecanismos que explotar. Su último estudio, publicado la semana pasada en Nature Communications, revela posibles nuevas dianas terapéuticas viables en el cáncer.
Los microtúbulos sufren diversas modificaciones en diferentes tipos de células y tejidos que meticulosamente definen sus funciones específicas. En este trabajo, el equipo científico vio que la Tubulina Tirosina Ligasa probable 11, también conocida como TTLL11, es una enzima que modifica los microtúbulos del huso. Específicamente, la enzima agrega cadenas de glutamato a la superficie de los microtúbulos. Este es un proceso conocido como poliglutamilación.
Descubrieron que la poliglutamilación de los microtúbulos define el dinamismo y la estabilidad de los microtúbulos del huso, lo que a su vez asegura la correcta segregación de los cromosomas. Las imágenes secuenciales revelaron que sin TTLL11, las células y los embriones de pez cebra tenían muchas más probabilidades de sufrir errores de segregación cromosómica.
Cuando examinaron los niveles de TTLL11 en el cáncer, en comparación con el tejido sano, mediante datos del Cancer Genome Atlas, una base de datos pública que incluye características moleculares de más de 20.000 cánceres primarios emparejados con muestras normales que abarcan 33 tipos de cáncer, encontraron que TTLL11 estaba significativamente regulado a la baja en cada uno de estos tumores en comparación con el tejido normal correspondiente.
“Encontramos que los niveles bajos de TTLL11 son altamente específicos para el cáncer. Esto es emocionante porque desvela otra fase que describe cómo se regulan los microtúbulos durante la división celular en el cáncer. Los fármacos que interfieren con la dinámica de los microtúbulos ya son una de las terapias de primera línea más exitosas contra el cáncer. Si esto resulta ser una nueva diana terapéutica que sea viable, nuestros hallazgos allanan el camino para la creación de una nueva generación de fármacos más precisos y efectivos que los tratamientos convencionales”, explica la Dra. Vernos.
Los autores del estudio también explicaron por qué los niveles bajos de TTLL11 afectan a la división celular. “Los microtúbulos deben establecer conexiones estables con los cromosomas para alinearlos y separarlos. Estas conexiones también deben ser lo suficientemente flexibles para corregirse a tiempo y evitar errores durante la segregación. Los microtúbulos en las células cancerosas tienen niveles bajos de TTLL11. Esto hace que los microtúbulos sean demasiado inflexibles, favoreciendo la segregación de los cromosomas sin errores corregidos, que resultarán en células aneuploides. Queda por demostrar si este es un mecanismo explotado por las células cancerosas para crecer y generar diversidad a través de los errores aleatorios de segregación cromosómica. Esto constituye nuevas e interesantes vías de investigación”, concluye la Dra. Vernos.
La investigación se publica en Nature Communications y está dirigida por el primer autor Iván Zadra y la autora principal Dra. Isabelle Vernos en el CRG. Entre los colaboradores se encuentran los Profesores de Investigación ICREA Dra. Verena Ruprecht y Dr. Luis Serrano, también en el CRG, así como a Carsten Janke en el Institut Curie. Entre los autores se encuentran Senda Jiménez, Miquel Anglada, Carolina Segura y Zachary Compton.
EN CATALÀ
Un enzim del procés de divisió cel·lular identificada com a potencial nova diana terapèutica per al càncer
- Un equip científic ha identificat un enzim que evita que les cèl·lules cometin errors durant la divisió cel·lular, garantint que els cromosomes puguin separar-se correctament
- La recerca ha descobert que l’activitat de l’enzim està compromesa en les cèl·lules canceroses humanes, aplanant el camí per a què futures investigacions explorin si el càncer s’aprofita del mecanisme per a créixer
- L’equip científic del CRG, que publica els resultats de l’estudi a Nature Communications, durà a terme futurs estudis per saber si l’enzim és una possible diana terapèutica viable en el càncer
Per a crear noves cèl·lules, les existents han de dividir-se. Aquest és un procés continu, freqüent i ubic que comença a la concepció i acaba amb la mort. S’estima que hi ha 37 bilions de cèl·lules en els teixits i òrgans del cos humà, cadascuna de les quals s’origina a partir d’una cèl·lula que es divideix en dos.
Quan la divisió cel·lular falla, pot provocar la creació de noves cèl·lules amb un nombre anormal de cromosomes, un fenomen conegut com aneuploïdia. La freqüència amb què es produeixen els errors de segregació cromosòmica es coneix com a inestabilitat cromosòmica (CIN). En alguns casos, per exemple, en un embrió en desenvolupament, això pot promoure l’avortament espontani i, en d’altres, pot contribuir a malalties humanes com el càncer. L’aneuploïdia i la CIN són trets comuns en els tumors particularment agressius.
S’estudia la divisió cel·lular per a comprendre com es produeix la segregació cromosòmica sense errors cada cop que una cèl·lula es divideix. També s’investiga per què i com poden produir-se els errors que generen les cèl·lules aneuploides.
Una segregació cromosòmica fidel depèn totalment de la unió correcta entre els cromosomes i el fus mitòtic, la maquinària molecular que empeny els cromosomes cap als extrems oposats d’una cèl·lula. El fus està format per microtúbuls, tubs buits llargs formats per proteïnes. Els microtúbuls han de mantenir-se suficientment estables per moure i alinear els cromosomes, però també suficientment dinàmics per permetre la correcció de les unions errònies abans què els cromosomes se separin i se segreguin.
Aquesta dinàmica dels microtúbuls i la seva precisa regulació són processos fonamentals per a comprendre com es divideixen les cèl·lules. La seva importància es destaca per la identificació d’un compost a principis de la dècada de 1970 que encara s’usa actualment en la quimioteràpia. El tractament estabilitza directament els microtúbuls, fet que permet que les cèl·lules canceroses s’autodestrueixin.
Per a la Professora d’Investigació ICREA Isabelle Vernos, cap de grup al programa de recerca de Biologia Cel·lular Quantitativa al Centre de Regulació Genòmica (CRG), encara no es compren completament com es regula la dinàmica dels microtúbuls durant la divisió cel·lular en el càncer. Una major comprensió podria revelar nous mecanismes per explotar. El seu darrer estudi, publicada la setmana passada a Nature Communications, desvela possibles noves dianes terapèutiques viables en el càncer.
Els microtúbuls pateixen diverses modificacions en diferents tipus de cèl·lules i teixits que meticulosament defineixen les seves funcions específiques. En aquest treball, l’equip científic veié que la Tubulina Tirosina Ligasa probable 11, també coneguda com a TTLL11, és un enzim que modifica els microtúbuls del fus. Específicament, l’enzim agrega cadenes de glutamat a la superfície dels microtúbuls. Aquest és un procés conegut com a poliglutamilació.
Descobriren que la poliglutamilació dels microtúbuls defineix el dinamisme i l’estabilitat dels microtúbuls del fus, fet que alhora assegura la correcta segregació dels cromosomes. Les imatges seqüencials revelaren que sense TTLL11, les cèl·lules i els embrions de peix zebra tenien moltes més probabilitats de patir errors de segregació cromosòmica.
Quan examinaren els nivells de TTLL11 en el càncer, en comparació amb el teixit sa, mitjançant dades del Cancer Genome Atlas, una base de dades pública que inclou característiques moleculars de més de 20.000 càncers primaris emparellats amb mostres normals que comprenen 33 tipus de càncer, trobaren que TTLL11 estava significativament regulat a la baixa en cadascun d’aquests tumors en comparació amb el teixit normal corresponent.
“Trobàrem que els nivells baixos de TTLL11 són altament específics per al càncer. Això és emocionant perquè desvela una fase que descriu com es regulen els microtúbuls durant la divisió cel·lular en el càncer. Els fàrmacs que interfereixen amb la dinàmica dels microtúbuls ja són una de les teràpies de primera línia més exitoses contra el càncer. Si això resulta ésser una nova diana terapèutica que sigui viable, les nostres troballes aplanen el camí per a la creació d’una nova generació de fàrmacs més precisos i efectius que els tractaments convencionals”, explica la Dra. Vernos.
Els autors de l’estudi també explicaren per què els nivells baixos de TTLL11 afecten la divisió cel·lular. “Els microtúbuls han d’establir connexions estables amb els cromosomes per alinear-los i separar-los. Aquestes connexions també han de ser suficientment flexibles per corregir-se a temps i evitar errors durant la segregació. Els microtúbuls en les cèl·lules canceroses tenen nivells baixos de TTLL11. Això fa que els microtúbuls siguin massa inflexibles, afavorint la segregació dels cromosomes sense errors corregits, que resultaran en cèl·lules aneuploides. Queda demostrar si aquest és un mecanisme explotat per les cèl·lules canceroses per a créixer i generar diversitat a través dels errors aleatoris de segregació cromosòmica. Això constitueix noves i interessants vies de recerca”, conclou la Dra. Vernos.
La recerca es publica a Nature Communications i està dirigida per el primer autor Iván Zadra i l'autora principal la Dra. Isabelle Vernos al CRG. Entre els col·laboradors s’hi troben els Professors d’Investigació Verena Ruprecht i Luis Serrano, també al CRG, així com Carsten Janke a l’Institut Curie. Entre els autors s’hi compten Senda Jiménez, Miquel Anglada, Carolina Segura i Zachary Compton.