NEWS
NEWS
Cancer has a unique nuclear metabolic fingerprint
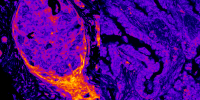
Breast cancers (left) show higher nuclear levels of energy-producing enzymes than lung cancers (right), revealing tissue-specific nuclear metabolism. Credit: Alberto Coll Manzano/Centro de Regulación Genómica
More than two hundred metabolic enzymes, many of which are normally tasked with producing energy in the mitochondria, are also found sitting directly on top of human DNA, according to a study published today in Nature Communications.
The research shows that different cell types, tissues and even cancers each have a unique pattern of metabolic enzymes compartmentalised inside the nucleus and interacting with DNA. It’s the first evidence of human cells having what the authors of the study call a “nuclear metabolic fingerprint”.
Though further work needs to be done to clarify whether the enzymes are catalysing reactions, turning genes on or off or simply providing structural support, the research provides new clues for how different types of tumours grow, adapt or resist treatment.
“Many of these enzymes synthesize essential building blocks of life, and their nuclear localization is associated with DNA repair. Their presence in the nucleus may therefore directly shape how cancer cells respond to genotoxic stress, a hallmark of many chemotherapeutic treatments. It’s an entirely new world to explore,” says Dr. Sara Sdelci, corresponding author of the study and researcher at the Centre for Genomic Regulation.
The team made the discovery by using a method that isolates proteins physically attached to chromatin, the natural state of DNA in human cells. They studied 44 cancer cell lines and 10 healthy cell types from ten different tissues.
Metabolism and genome regulation are traditionally thought to be occasionally porous, but generally separate systems. The nucleus hosts the genome while metabolic enzymes generate energy for cells in the mitochondria and cytoplasm.
That’s why the researchers were surprised with the scale of their discovery, which found that metabolic enzymes appear to be active participants in nuclear biology. 7% of all proteins found attached to chromatin were metabolic enzymes, suggesting the nucleus has its own independent ‘mini metabolism’.
Some of the enzymes were particularly unexpected. The team identified components of oxidative phosphorylation, the process that generates most of the cell’s energy, as regular residents in the human nucleus.
The absence, presence and abundance of the enzymes differed by cancer type. For example, oxidative phosphorylation enzymes were common in breast cancer cells but largely absent in lung cancer cells. When they examined tumour samples from patients, the authors of the study saw a similar pattern, demonstrating the tissue and disease-specific nature of nuclear metabolism.
“We’ve been treating metabolism and genome regulation as two separate universes, but our work suggests they’re talking to each other, and cancer cells might be exploiting these conversations to survive,” says Dr. Savvas Kourtis, first author of the study.
The researchers carried out experiments to figure out what some of the metabolic enzymes are doing. They studied one group of enzymes which provide building blocks for DNA synthesis and repair and found they gather around chromatin when DNA is damaged, helping repair the genome.
During these experiments they discovered that location matters. The enzyme IMPDH2 showed completely different behaviour depending on where it was. When the researchers forced it to stay only in the nucleus, it helped maintain genome stability, but when confined to the cytoplasm, it affected other pathways instead.
The discovery raises new questions about how cancer treatments work. Some drugs target a cancer’s metabolic activity, while others target its DNA repair mechanisms. If the two systems are more closely linked than previously thought, it has important implications for cancer research.
“It could help explain why tumours of different origins, even when carrying the same mutations, often respond very differently to chemotherapy, radiotherapy, or targeted inhibitors,” says Dr. Sdelci.
According to the authors of the study, their research is the first global evidence that the nucleus is crowded with metabolic enzymes. In the long run, mapping the location and function of the enzymes could help identify new biomarkers for diagnosis or new vulnerabilities that anti-cancer drugs could exploit.
But to do that researchers have to first determine what each enzyme is doing or whether all of them are even active. “Each enzyme may have its own, unique nuclear function, so this must be addressed one by one,” says Dr. Kourtis.
Another mystery is how enzymes get through the barrier between the nucleus and the cell cytoplasm in the first place. Many of the enzymes found on DNA are far larger than what the nuclear pore is normally thought to allow through, yet enormous bulky enzymes somehow make it through.
That raises new questions about which yet-to-be-discovered mechanism the cell is using to bypass the usual size limits. Following this line of inquiry could in turn lead to very precise therapeutic targets for controlling nuclear metabolic activity in diseased cells.
EN CASTELLANO
Descubren más de 200 enzimas del metabolismo en el núcleo de las células cancerosas
Más de doscientas enzimas metabólicas, muchas de las cuales se encargan habitualmente de producir energía en las mitocondrias, también se encuentran directamente asociadas al ADN humano en el núcleo de la célula, según un estudio publicado hoy en Nature Communications.
La investigación demuestra que distintos tipos celulares, tejidos e incluso distintos cánceres presentan un patrón único de enzimas metabólicas compartimentadas en el interior del núcleo que interactúan con el ADN. Se trata de la primera evidencia que indica que las células humanas poseen una “huella metabólica nuclear”.
Aunque será necesario seguir investigando para aclarar si estas enzimas catalizan reacciones, activan o desactivan genes o simplemente proporcionan apoyo estructural, los resultados apuntan a formas completamente nuevas en las que distintos tipos de tumores crecen, se adaptan o se hacen resistentes a los tratamientos.
“Muchas de estas enzimas sintetizan componentes esenciales para la vida y su localización nuclear se asocia a la reparación del ADN. Su presencia en el núcleo podría, por tanto, moldear directamente la forma en que las células cancerosas responden al estrés genotóxico, una característica de muchos tratamientos quimioterápicos. Es un mundo completamente nuevo por explorar”, afirma la doctora Sara Sdelci, autora principal del estudio e investigadora del Centro de Regulación Genómica.
El equipo realizó el hallazgo mediante un método que permite aislar proteínas físicamente unidas a la cromatina, el estado natural del ADN en las células humanas. Para ello se analizaron 44 líneas celulares de cáncer y 10 tipos celulares sanos procedentes de diez tejidos distintos.
Tradicionalmente, el metabolismo y la regulación del genoma se han considerado sistemas ocasionalmente permeables, pero en general separados. El núcleo alberga el genoma, mientras que las enzimas metabólicas generan energía para la célula en las mitocondrias y el citoplasma.
Por este motivo, la magnitud del descubrimiento sorprendió al equipo, que observó que las enzimas metabólicas parecen ser participantes activas de la biología nuclear. El 7 % de todas las proteínas encontradas asociadas a la cromatina eran enzimas metabólicas, lo que sugiere que el núcleo dispone de una especie de “mini metabolismo” propio e independiente.
Algunas de las enzimas identificadas resultaron especialmente inesperadas. El equipo detectó componentes de la fosforilación oxidativa, el proceso que genera la mayor parte de la energía celular, como residentes habituales del núcleo humano.
La ausencia, presencia y abundancia de estas enzimas variaba en función del tipo de cáncer. Por ejemplo, las enzimas de la fosforilación oxidativa eran frecuentes en células de cáncer de mama, pero estaban prácticamente ausentes en células de cáncer de pulmón. Cuando se analizaron muestras tumorales de pacientes, se observó un patrón similar, lo que pone de manifiesto el carácter específico del tejido y de la enfermedad de este metabolismo nuclear.
“Hemos tratado el metabolismo y la regulación del genoma como dos universos separados, pero nuestro trabajo sugiere que están en constante comunicación, y que las células cancerosas podrían estar explotando estas conversaciones para sobrevivir”, señala el doctor Savvas Kourtis, primer autor del estudio.
El equipo llevó a cabo experimentos para averiguar qué hacen algunas de estas enzimas metabólicas. Se estudió un grupo de enzimas que aportan las piezas de construcción necesarias para la síntesis y la reparación del ADN, y se observó que se agrupan alrededor de la cromatina cuando el ADN sufre daños, contribuyendo a la reparación del genoma.
Durante estos experimentos se descubrió, además, que la localización es determinante. La enzima IMPDH2 mostró comportamientos completamente distintos según su ubicación. Cuando se forzó a permanecer exclusivamente en el núcleo, ayudó a mantener la estabilidad del genoma; cuando se confinó al citoplasma, afectó a otras vías celulares diferentes.
El descubrimiento plantea nuevas preguntas sobre el funcionamiento de los tratamientos contra el cáncer. Algunos fármacos se dirigen a la actividad metabólica del tumor, mientras que otros actúan sobre los mecanismos de reparación del ADN. Si ambos sistemas están más estrechamente ligados de lo que se pensaba hasta ahora, las implicaciones para la investigación oncológica son relevantes.
“Podría ayudar a explicar por qué tumores de orígenes distintos, incluso cuando comparten las mismas mutaciones, responden de forma muy diferente a la quimioterapia, la radioterapia o los inhibidores dirigidos”, añade la doctora Sdelci.
La investigación constituye la primera evidencia global de que el núcleo está densamente poblado por enzimas metabólicas. A largo plazo, cartografiar la localización y la función de estas enzimas podría ayudar a identificar nuevos biomarcadores para el diagnóstico o nuevas vulnerabilidades que los fármacos contra el cáncer podrían explotar.
No obstante, para ello será necesario determinar primero qué función desempeña cada enzima o incluso averiguar si todas ellas están activas. “Cada enzima puede tener su propia función nuclear específica, por lo que esto deberá abordarse caso por caso”, afirma el doctor Kourtis.
Otro de los enigmas que plantea el estudio es cómo estas enzimas atraviesan la barrera que separa el núcleo del citoplasma celular. Muchas de las enzimas encontradas en el ADN son mucho más grandes de lo que normalmente se considera que permite el poro nuclear, y, sin embargo, estas voluminosas proteínas consiguen acceder al núcleo.
Esto plantea nuevas preguntas sobre qué mecanismos desconocidos utiliza la célula para sortear los límites habituales de tamaño. Seguir esta línea de investigación podría conducir, a su vez, a dianas terapéuticas muy precisas para controlar la actividad metabólica nuclear en células enfermas.
EN CATALÀ
Descobreixen més de 200 enzims del metabolisme al nucli de les cèl·lules canceroses
Més de dos-cents enzims metabòlics, molts dels quals s'encarreguen habitualment de produir energia a les mitocòndries, també es troben directament associats a l'ADN humà en el nucli de la cèl·lula, segons un estudi publicat avui a Nature Communications.
La investigació demostra que diferents tipus cel·lulars, teixits i fins i tot diferents càncers presenten un patró únic d'enzims metabòlics compartimentats a l'interior del nucli que interactuen amb l'ADN. Es tracta de la primera evidència que indica que les cèl·lules humanes posseeixen una "empremta metabòlica nuclear".
Tot i que caldrà continuar investigant per aclarir si aquests enzims catalitzen reaccions, activen o desactiven gens o simplement proporcionen suport estructural, els resultats apunten a formes completament noves en què diferents tipus de tumors creixen, s'adapten o es fan resistents als tractaments.
"Molts d'aquests enzims sintetitzen components essencials per a la vida i la seva localització nuclear s'associa a la reparació de l'ADN. La seva presència al nucli podria, per tant, modelar directament la forma en què les cèl·lules canceroses responen a l'estrès genotòxic, una característica de molts tractaments quimioteràpics. És un món completament nou per explorar", afirma la doctora Sara Sdelci, autora principal de l'estudi i investigadora del Centre de Regulació Genòmica.
L'equip va realitzar la troballa mitjançant un mètode que permet aïllar proteïnes físicament unides a la cromatina, l'estat natural de l'ADN en les cèl·lules humanes. Per a això es van analitzar 44 línies cel·lulars de càncer i 10 tipus cel·lulars sans procedents de deu teixits diferents.
Tradicionalment, el metabolisme i la regulació del genoma s'han considerat sistemes ocasionalment permeables, però en general separats. El nucli alberga el genoma, mentre que els enzims metabòlics generen energia per a la cèl·lula a les mitocòndries i el citoplasma.
Per aquest motiu, la magnitud del descobriment va sorprendre l'equip, que va observar que els enzims metabòlics semblen ser participants actius de la biologia nuclear. El 7% de totes les proteïnes trobades associades a la cromatina eren enzims metabòlics, la qual cosa suggereix que el nucli disposa d'una espècie de "mini metabolisme" propi i independent.
Alguns dels enzims identificats van resultar especialment inesperats. L'equip va detectar components de la fosforilació oxidativa, el procés que genera la major part de l'energia cel·lular, com a residents habituals del nucli humà.
L'absència, presència i abundància d'aquests enzims variava en funció del tipus de càncer. Per exemple, els enzims de la fosforilació oxidativa eren freqüents en cèl·lules de càncer de mama, però estaven pràcticament absents en cèl·lules de càncer de pulmó. Quan es van analitzar mostres tumorals de pacients, es va observar un patró similar, fet que posa de manifest el caràcter específic del teixit i de la malaltia d'aquest metabolisme nuclear.
"Hem tractat el metabolisme i la regulació del genoma com dos universos separats, però el nostre estudi suggereix que estan en constant comunicació, i que les cèl·lules canceroses podrien estar explotant aquestes converses per sobreviure", assenyala el doctor Savvas Kourtis, primer autor de l'estudi.
L'equip va dur a terme experiments per esbrinar què fan alguns d'aquests enzims metabòlics. Es va estudiar un grup d'enzims que aporten les peces de construcció per a la síntesi i la reparació de l'ADN, i es va observar que s'agrupen al voltant de la cromatina quan l'ADN pateix danys, contribuint a la reparació del genoma.
Durant aquests experiments es va descobrir, a més, que la localització és determinant. L'enzim IMPDH2 va mostrar comportaments completament diferents segons la seva ubicació. Quan es va forçar a romandre exclusivament al nucli, va ajudar a mantenir l'estabilitat del genoma; quan es va confinar el citoplasma, va afectar altres vies cel·lulars diferents.
El descobriment planteja noves preguntes sobre el funcionament dels tractaments contra el càncer. Alguns fàrmacs es dirigeixen a l'activitat metabòlica del tumor, mentre que d'altres actuen sobre els mecanismes de reparació de l'ADN. Si ambdós sistemes estan més estretament lligats del que es pensava fins ara, les implicacions per a la investigació oncològica són rellevants.
"Podria ajudar a explicar per què tumors d'orígens diferents, fins i tot quan comparteixen les mateixes mutacions, responen de forma molt diferent a la quimioteràpia, la radioteràpia o els inhibidors dirigits", afegeix la doctora Sdelci.
La investigació constitueix la primera evidència global que el nucli està densament poblat per enzims metabòlics. A llarg termini, la localització i la funció d'aquests enzims podria ajudar a identificar nous biomarcadors per al diagnòstic o noves vulnerabilitats que els fàrmacs contra el càncer podrien explotar.
No obstant això, per a això serà necessari determinar primer quina funció exerceix cada enzim o fins i tot esbrinar si tots estan actius. "Cada enzim pot tenir la seva pròpia funció nuclear específica i, per tant, això s'haurà d'abordar cas per cas", afirma el doctor Kourtis.
Un altre dels enigmes que planteja l'estudi és com aquests enzims travessen la barrera que separa el nucli del citoplasma cel·lular. Molts dels enzims trobats en l'ADN són molt més grans del que normalment es considera que permet el por nuclear, i, no obstant això, aquestes voluminoses proteïnes aconsegueixen accedir al nucli.
Això planteja noves preguntes sobre quins mecanismes desconeguts utilitza la cèl·lula per sortejar els límits habituals de mida. Seguir aquesta línia d'investigació podria conduir, alhora, a dianes terapèutiques molt precises per controlar l'activitat metabòlica nuclear en cèl·lules malaltes.