Act of sabotage determines mammalian embryonic development
Act of sabotage determines mammalian embryonic development
Act of sabotage determines mammalian embryonic development
Alternative splicing is a fundamental biological process that allows cells to make many different types of mRNAs and proteins from a limited number of genes. For many animals, including humans, it is a feature that is essential for the development of complex cells such as muscles or neurons.
Its fundamental importance means that alternative splicing is a very tightly regulated process. But a new study published today in the journal Science Advances has found evidence that the regulation of alternative splicing, which rarely goes wrong in healthy cells, goes haywire in an unexpected place – the cells of a newly formed embryo.
Researchers at the Centre for Genomic Regulation (CRG) in Barcelona made the discovery after creating an atlas of splicing events during the early development of cows, humans and mice.
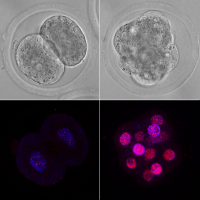
They found that when human embryos are balls of just 8 cells, they express a huge variety of alternative mRNAs, so much so that the splicing diversity was the highest ever recorded across any cell or tissue studied to date. When the embryos transitioned to the next stage of development, their splicing activity returned to normal.
According to the authors of the study, this is evidence that the regulation of alternative splicing collapses temporarily at a crucial stage of development known as zygotic genome activation. This is when an early embryo transitions from using maternal resources such as proteins and RNA and making its own.
Importantly, the researchers believe the newly-discovered phenomenon occurs because it is developmentally programmed – a purposeful act of sabotage. “We think this happens because there are instructions in our genome that tell a few genes to not do their job at that developmental stage. The embryo cells mess up their splicing on purpose and they do so for a functional reason,” says ICREA Research Professor Manuel Irimia, senior author of the study.
An important clue for why the regulation of splicing fails at this crucial moment lies in the function of the proteins affected. The researchers found that splicing failure destroyed proteins responsible for responding to DNA damage.
“We saw that the DNA damage response at this stage of development was low. While splicing failure isn’t the only factor affecting this defense mechanism, it’s partly responsible for destroying the proteins involved. We don’t know why this happens, but it’s possibly because transcription itself carries a risk of DNA damage. As embryos activate their genome for the first time and start to transcribe, there may be trade-offs involved in order to avoid developmental failure.” says Dr. Barbara Pernaute, postdoctoral researcher at the CRG and co-first author of the study.
According to Dr. Pernaute, these results improve our understanding of how embryos develop during these early stages and could open doors for improvements in assisted reproductive technologies.
The findings could also be useful for advancing research efforts in the creation of totipotent cells from stem cells, a long-term aspiration for regenerative medicine. As these early embryonic cells are truly totipotent cells, knowledge of the mechanism could lead to advances that reverse engineer stem cells to induce totipotency.
“Recent studies carried out by other research groups around the world have shown that artificially inducing the mechanism we find in our study transforms stem cells into totipotent cells. We believe these programmed splicing failures also occur in other physiological contexts. We are only just scratching the surface for the importance this mechanism has for biological processes”, concludes Dr. Irimia.
EN CASTELLANO
Un acto de sabotaje determina el desarrollo embrionario de los mamíferos
El empalme alternativo es un proceso biológico fundamental que permite a las células crear muchos tipos diferentes de ARNm y proteínas a partir de un número limitado de genes. Para muchos animales, incluidos los humanos, es un proceso vital para el desarrollo de células complejas como los músculos o las neuronas.
Dada su importancia fundamental, el empalme alternativo es un proceso estrictamente regulado. Pero un nuevo estudio publicado hoy en la revista Science Advances ha evidenciado que la regulación del empalme alternativo, que casi nunca falla en las células sanas, se descontrola en un lugar inesperado: las células de un embrión recién formado.
Un equipo científico del Centro de Regulación Genómica (CRG), en Barcelona, descubrió el fenómeno después de crear un atlas de eventos de empalme durante el desarrollo temprano de vacas, humanos y ratones.
Descubrieron que cuando los embriones humanos son bolas de solo 8 células, expresan una gran variedad de ARNm alternativos. Tanta, que la diversidad de empalme fue la más alta jamás registrada en cualquier célula o tejido estudiado hasta la fecha. Cuando los embriones pasaron a la siguiente etapa de desarrollo, su actividad de empalme volvió a la normalidad.
Según los autores del estudio, esto evidencia que la regulación del empalme alternativo colapsa temporalmente en una etapa crucial del desarrollo conocida como activación del genoma cigótico. Esto es, cuando un embrión temprano pasa de usar proteínas y ARN maternos a fabricar los suyos propios.
El equipo cree que el nuevo fenómeno ocurre porque está programado durante el desarrollo, es decir, es un acto deliberado de sabotaje. “Creemos que esto sucede porque hay instrucciones en nuestro genoma que le dicen a algunos genes que no hagan su trabajo en esta etapa de desarrollo. Las células del embrión estropean su empalme a propósito y lo hacen por una razón funcional”, afirma el profesor de investigación ICREA Manuel Irimia, autor principal del estudio.
Una pista importante de por qué falla la regulación del empalme radica en la función de las proteínas afectadas. El equipo evidenció que el fracaso de la regulación del empalme destruye las proteínas responsables de responder al daño del ADN.
“Vimos que la respuesta al daño del ADN en esta etapa de desarrollo era baja. Si bien el fracaso de la regulación del empalme no es el único factor, es en parte responsable de la destrucción de las proteínas involucradas en este mecanismo de defensa. No sabemos por qué sucede esto, pero posiblemente se deba a que la transcripción en sí conlleva un riesgo de daño al ADN. A medida que los embriones activan su genoma por primera vez y comienzan a transcribirse, puede haber compensaciones involucradas para evitar fallos en el desarrollo”, afirma la Dra. Barbara Pernaute, investigadora postdoctoral en el CRG y coautora del estudio.
Según la Dra. Pernaute, estos resultados mejoran nuestra comprensión de cómo se desarrollan los embriones durante estas primeras etapas y podrían abrir puertas para mejoras en las tecnologías de reproducción asistida.
Los hallazgos también podrían ser útiles para avanzar en los esfuerzos de investigación en la creación de células totipotentes a partir de células madre, una aspiración a largo plazo para la medicina regenerativa. Dado que estas células embrionarias tempranas son realmente células totipotentes, el conocimiento del mecanismo podría conducir a avances que utilicen ingeniería inversa para inducir la totipotencia en células madre.
“Estudios recientes llevados a cabo por otros grupos de investigación en otras partes del mundo han demostrado que la inducción artificial del mecanismo que encontramos en nuestro estudio transforma las células madre en células totipotentes. Creemos que el fracaso programado de la regulación del empalme también ocurre en otros contextos fisiológicos. Apenas estamos desglosando la importancia que tiene este mecanismo para los procesos biológicos”, concluye el Dr Irimia.
EN CATALÀ
Un acte de sabotatge determina el desenvolupament embrionari dels mamífers
L’empalmament alternatiu és un procés biològic fonamental que permet a les cèl·lules crear molts tipus diferents d’ARNm i proteïnes a partir d’un número limitat de gens. Per a molts animals, inclosos els humans, és un procés vital per al desenvolupament de cèl·lules complexes, com els músculs o les neurones.
Donada la seva importància fonamental, l’empalmament alternatiu és un procés estrictament regulat. Però un nou estudi publicat avui a la revista Science Advances ha evidenciat que la regulació de l’empalmament alternatiu, que no falla gairebé mai a les cèl·lules sanes, es descontrola en un lloc inesperat: les cèl·lules d’un embrió acabat de formar.
Un equip científic del Centre de Regulació Genòmica (CRG), a Barcelona, descobrí el fenomen després de crear un atles d’esdeveniments d’empalmament durant el desenvolupament primerenc de vaques, humans i ratolins.
Descobriren que quan els embrions humans són boles de només 8 cèl·lules, expressen una gran varietat d’ARNm alternatius. Tanta, que la diversitat de l’empalmament fou la més alta registrada mai abans en qualsevol cèl·lula o teixit estudiat fins a l’actualitat. Quan els embrions passaren a la següent etapa de desenvolupament, la seva activitat d’empalmament tornà a la normalitat.
Segons els autors de l’estudi, això evidencia que la regulació de l’empalmament alternatiu col·lapsa temporalment en una etapa crucial del desenvolupament, coneguda com a activació de genoma zigòtic. És a dir, quan un embrió primerenc passa d’emprar proteïnes i ARN materns a fabricar els seus propis.
L’equip creu que el nou fenomen es produeix perquè està programat durant el desenvolupament, és a dir, és un acte deliberat de sabotatge. “Creiem que això passa perquè hi ha instruccions al nostre genoma que li diuen a alguns gens que no facin la seva feina en aquesta etapa del desenvolupament. Les cèl·lules de l’embrió fan malbé el seu empalmament expressament i ho fan per una raó funcional”, afirma el professor d’investigació ICREA Manuel Irimia, autor principal de l’estudi.
Una pista important de per què falla la regulació de l’empalmament radica en la funció de les proteïnes afectades. L’equip evidencià que el fracàs de la regulació de l’empalmament destrueix les proteïnes responsables de respondre al dany de l’ADN.
“Vam veure que la resposta al dany de l’ADN en aquesta etapa del desenvolupament era baixa. Si bé el fracàs de la regulació de l’empalmament no és l’únic factor, és en part responsable de la destrucció de les proteïnes involucrades en aquest mecanisme de defensa. No sabem per què passa això, però possiblement sigui perquè la transcripció en si mateixa comporta un risc de dany a l’ADN. A mesura que els embrions activen el seu genoma per primer cop, i comencen a transcriure’s, pot haver-hi compensacions involucrades per evitar fallades en el desenvolupament”, afirma la Dra. Barbara Pernaute, investigadora postdoctoral al CRG i coautora de l’estudi.
Segons la Dra. Pernaute, aquests resultats milloren la nostra comprensió de com es desenvolupen els embrions durant aquestes primeres etapes i podrien obrir portes per millorar les tecnologies de reproducció assistida.
Les troballes també podrien ser útils per avançar en els esforços de la recerca en la creació de cèl·lules totipotents a partir de cèl·lules mare, una aspiració a llarg termini per a la medicina regenerativa. Tenint en compte que aquestes cèl·lules embrionàries primerenques són realment cèl·lules totipotents, el coneixement del mecanisme podria conduir a avenços que emprin l’enginyeria inversa per a induir la totipotència en cèl·lules mare.
“Estudis recents duts a terme per d’altres grups de recerca en d’altres parts del món han demostrat que la inducció artificial del mecanisme que trobem en el nostre estudi transforma les cèl·lules mare en cèl·lules totipotents. Creiem que el fracàs programat de la regulació de l’empalmament es produeix en d’altres contextos fisiològics. Tot just estem desglossant la importància que té aquest mecanisme per als processos biològics”, conclou el Dr. Irimia.